北京北纳创联生物技术研究院
14 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
培养基的灵敏度检查(促菌生长性)
6878 人阅读发布时间:2016-04-21 17:22
培养基灵敏度(促菌生长性)的重要性在于:在规定的试验条件下,培养基如果不能支持微生物的生长,那么检品中可能存在的微生物将不能在该培养基内或培养基表面生长至出现浑浊或形成菌落,从而导致实验的假阴性结果。为确保培养基灵敏度(促菌生长性)的可靠,灵敏度试验应傲双份检查,并且使用低菌接种量至关重要,菌接种量一定要控制在100个CFU以内。
(一)中国药典2005版对无菌检查用培养基的灵敏度检查方法要求对所购的每个批号的脱水培养基进行灵敏度检查:
1.取金黄色葡萄球菌、藤黄微球菌的营养琼脂斜面新鲜培养物,及产芽胞梭菌的需气菌、厌气菌液体培养基新鲜培养物,无菌操作,用 0.9%无菌氯化钠溶液制成均匀的菌悬液。分别取上述菌悬液 1ml,加入 0.9% 无菌氯化钠溶液 9ml 中作10倍系列稀释,至制成每毫升中含 10~100个菌(CFU)的供试稀释菌液(含菌量用平皿菌数计数法确定)。
2.取白色念珠菌及黑曲菌的真菌琼脂培养基斜面新鲜培养物,同上操作至制成每毫升中含10~100个菌(CFU)的供试稀释菌液。(含菌量用平皿菌数计数法确定)。
3.接种培养基 将由上述 “1” 制得的3种供试稀释菌液各 1ml,分别接种至每管装量为12ml 的硫乙醇酸盐液体培养基中各3管,以未接种的培养基3管作对照试验。置30~35℃培养3天,逐日记录结果。将由上述 “2” 制得的 2种供试稀释菌液各 lml,分别接种至每管装量为 9ml 的改良马丁液体培养基中各3管,以未接种的培养基3管作对照试验。置 20~25℃ 培养5天,逐日记录结果。
4.结果判定 以每株菌接种后的培养基不得少于2管呈现生长,即该培养基的促菌生长试验符合要求。
(二)美国药典对无菌检查用培养基的灵敏度检查方法 USP26 对无菌检查用培养基的灵敏度检查作如下规定:“对每个不同批号的脱水培养基均应进行灵敏度检查(促菌生长检查)。向每瓶培养基内分别接人试验菌种(表3—1),每瓶接种量小于 100个菌(CFU),每个菌种接种两瓶培养基,将接过种的培养基置于指定条件下培养。若在5天内可明显观察到培养基内有微生物生长,则证明此培养基合格。此试验也可与无菌检查试验同时进行,但是,一旦所用培养基不符合无菌要求或者不符合促菌生长(灵敏度)检查要求,无菌检查结果应视为无效。”
(三)微生物限度检查用培养基的灵敏度检查方法虽然微生物限度检查用培养基的灵敏度检查中国药典中尚未有规定。但是由于在实验中常常能发现国产培养基的质量问题,特别是在进口药品质量复核中同时用国产培养基和厂方提供的进口培养基检验时,菌落的大小、数量、需培养的时间均有很大差别。为保证微生物限度检查中菌数计数结果及控制菌检出的可靠性,药典对微生物限度检查用培养基的灵敏度检查应尽快提到议事日程上来。切实可行的简便方法如下:
1.用于菌数计数的半固体琼脂培养基促菌生长(灵敏度)检查的方法对每个不同批号的脱水培养基均应进行灵敏度检查(促菌生长检查)。取预先制备好的琼脂培养基平皿 3.5 个,用表面涂布法每块平板表面接种 30~100 个试验菌,同时用已知质量保证的同型号培养基平皿3.5个(如较著名的如MERCK,DIFICOL 产品)做对照试验,待培养基表面的菌液被琼脂培养基吸干或风干后,将培养皿倒置于培养基的使用温度下培养48~72小时,(也可采用浇碟法进行)取出培养后的平皿点计菌落数。样品培养基上的微生物数量应不得低于对照培养基上微生物生长数量的70%。否则,需重新检查,或该培养基被视为不符合促生长要求。
2.用于控制菌检查的富集培养基的促菌生长(灵敏度)检查的方法对每个不同批号的脱水培养基均应进行灵敏度检查(促菌生长检查)。可参照无菌检查用培养基灵敏度检查方法进行,每 100ml 培养基内分别接人试验菌小于 100个菌(CFU),每个菌种接种两瓶培养基,将接过种的培养基置于指定条件下培养。应在16~18小时后可明显观察到培养基内有敷生物生长,则证明此培养基合格。
原则上无论是采用脱水培养基还是按药典处方配制的培养基,一旦制成成品培养基,则应对每个配制批的培养基进行促菌生长(灵敏度检查)试验,以考察培养基的质量。按脱水培养基的生产批号做灵敏度检查是基于培养基的灭菌程序已经过验证。
如果实验室使用的是商购的成品型培养基,供应商应随培养基提供相应批次的培养基质量检测报告,报告包括培养基的 pH 值、无菌检查结果和促菌生长(灵敏度)试验结果等项目。笔者认为,在使用某一新的成品培养基(新供应商或新培养基品种)时,应至少考察三个不同批次的培养基质量,只有三批质量均合格方可使用该培养基。除无菌检查用培养基外。其他实验用成品培养基一旦初始确认合格后,可审查供应商的质检报告,而不必每批再作无菌检查和灵敏度检查,但每半年应至少检查一次,以复核其质量。用于无菌检查试验的每批培养基,均必须按药典规定进行灵敏度检查试验,此规定同样适用于实验室自行配制的培养基。
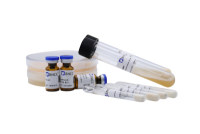
图3—1是法国生物梅里埃(Bio—Merieux)公司生产的用于无菌检查的成品培养基及淋洗液,其质量符合欧盟、美国及日本等国的药典要求。
建议在正式使用前即应完成对培养基、缓冲液和试剂的质量检查。如果在进行灵敏度试验的同时,也使用该培养基进行样品检查,那么,一旦培养基的无菌性或灵敏度试验不符合规定,则检验结果应无效。无论这些质量控制检查试验何时完成,实验室都必须在相关产品敦行之前或检验报告发出之前,对所用培养基、缓冲液和试剂的无菌性及灵敏度试验资料的完整性和合格结论予以确认。
灵敏度(促生长)检查试验用的菌悬液,可用药典规定的在5代之内的标准菌种制得,也可向具备适当资质的供应商购买。目前市场上的商用产品,如REMEL 公司的培养基质量 Quanti-cultR 检查用菌种,小瓶内每片薄膜上含有10~100 CFU。此类产品使用简单,但操作者需严格遵守供应商的使用要求。另外,尽管所购试验菌种均附有质量证书,正式使用前,仍必须用倾注平皿法或铺表面法等标准检测方法对菌悬液的微生物数量进行复核确认(表3—2)。
来源:北纳细胞网 www.bncc.org.cn